Fuerzas moleculares de los líquidos
Capilaridad
Se llaman tubos capilares (de capillus, cabello) unos tubos de diámetro muy pequeño. En esos tubos los líquidos no obedecen las leyes de los vasos comunicantes.
Se toma un tubo de vidrio que se sumerge en parte en un líquido, conservándolo vertical (ver figura 1). Si el tubo no es mojado por el líquido (mercurio), el nivel interior está más bajo que el exterior (ver figura 1, TT), lo que se llama depresión capilar. La superficie libre presenta un menisco convexo (a, b); entonces es la cohesión la que vence a la adherencia.

Figura 1: Tubos capilares
Si el tubo es mojado por el líquido (agua), el nivel en el interior del tubo está más alto que en el exterior (ver figura 1, MN), lo que se llama ascensión capilar. En este caso la superficie es cóncava (c, d) y la adherencia vence a la cohesión.
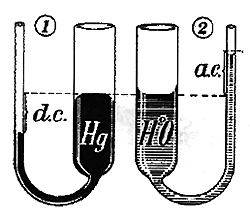
Figura 2: Depresiones y ascensiones capilares
La capilaridad desempeña un papel importante en la circulación vegetal, en la ascensión del aceite en las mechas de las lámparas y en la imbibición de los cuerpos porosos (esponja, azúcar, montón de arena, etc.).
La capilaridad explica que un líquido suba a alturas diferentes en dos tubos angostos de diámetros diferentes cuando se comunican libremente entre sí (ver figura 2).
En (1) existe una depresión capilar (dc): el mercurio no moja el tubo; mientras que en (2), como el agua moja el tubo, hay ascensión (ac) con relación al tubo más ancho.
El valor de la ascensión o depresión capilar depende solamente del diámetro de los tubos y obedece a la ley de Jurín.
Ley de Jurín
Para todo líquido contenido en tubos capilares de diámetros diferentes, las alturas del líquido en los diversos tubos son inversamente proporcionales a los diámetros de los mismos.

Figura 3: Ley de los diámetros (capilaridad)
Se comprueba fácilmente esta ley por el método de Gay-Lussac. Basta para ello colocar en un líquido tubos de diámetros diferentes abiertos en los dos extremos (ver figura 3). Con la ayuda de la varilla graduada (izquierda de la figura) se mide la ascensión en los varios tubos.
Dicha ascensión del agua es mayor en c que en b, por ser menor su diámetro; por la misma razón es mayor en b que en a.
Difusión
La difusión es el fenómeno por el cual dos líquidos miscibles, o dos gases cualesquiera, puestos en contacto, llegan a formar una mezcla homogénea en un plazo más o menos largo.
Ejemplos:
1º. Si en un vaso se colocan unos cristales de sulfato de cobre (azul) y se llena el vaso de agua, en el fondo se formará un líquido azul (solución del sulfato de cobre en el agua), que se mantendrá separado del resto del agua. Pero, si se guarda el vaso así preparado durante algunos días, aunque no se lo agite, se encontrará al fin en él un líquido azul homogéneo, producido por la difusión de los dos líquidos.

Figura 4: Ascensión del agua y depresión del mercurio entre dos láminas de vidrio muy juntas. La punta de líquido sube o baja en el ángulo tanto más cuanto menor se vuelve el ángulo.
2º. Se ponen en comunicación dos matraces (ver figura 5) que contengan CO2 el de abajo y H2 el de arriba; al cabo de algún tiempo, cada matraz contendrá una cantidad igual de cada gas. El gas más pesado es el menos difusible, es decir, emplea más tiempo para difundirse. La presión de la mezcla es igual a la suma de las presiones que tendría cada gas si ocupara todo el espacio.
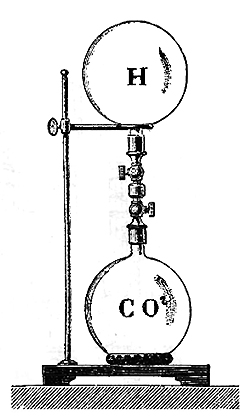
Figura 5: Difusión del hidrógeno (H2) con el CO2. (El CO2 es 22 veces más pesado que el H2).
Ósmosis
La ósmosis es el fenómeno por el cual dos líquidos miscibles, o dos gases, atraviesan las membranas porosas que los separan, para formar una mezcla homogénea.
En un recipiente de vidrio con agua A (ver figura 6) se sumerge un tubo B que contiene agua azucarada y cuyo fondo está cerrado por una membrana porosa C. Al cabo de algún tiempo los dos líquidos habrán filtrado; en efecto, el agua del vaso A estará azucarada y el nivel en el tubo B, que al principio bajó (exosmosis), alcanza después el nivel m (endósmosis).
Se llaman cristaloides a los líquidos que atraviesan las membranas (el azúcar) y coloides a los demás (clara de huevo, protoplasma). La ósmosis explica la absorción de la savia y de los alimentos.
Presión osmótica
Si se cierra la extremidad superior del tubo B (ver figura 6) por medio de un tapón que comunica con un manómetro (ver figura 7), se observa que durante el experimento el mercurio sube cada vez más en el manómetro y después permanece fijo, en el nivel n. Esto demuestra que el agua de A entra en B hasta que la compresión del aire en la parte superior del vaso B, que se transmite al mercurio del manómetro, adquiere un valor máximo. De aquí resulta que la presión (reacción) del aire comprimido sobre el vaso B impide una nueva entrada del agua.

Figura 6: Fenómeno de ósmosis

Figura 7: Presión osmótica
Esta presión, que hace subir el mercurio del manómetro, se llama presión osmótica.
La presión osmótica depende de la concentración de la disolución y de la temperatura. A temperatura constante, es proporcional a la concentración.
Si la temperatura está a tº, la presión es igual a la presión a 0º multiplicada por (1 + αt), es decir, el binomio de la dilatación de la disolución.
Presión a tº = Presión a 0º (1 + αt)
Tensión superficial
El estudio matemático de las fuerzas moleculares que se ejercen en la superficie libre de un líquido en equilibrio nos hace admitir que dicha superficie es comparable a una membrana elástica tensa, análoga a una membrana de caucho que tuviera tendencia a retraerse; luego:
La tensión superficial es la fuerza que atrae las moléculas de la superficie en el sentido de la superficie del líquido.
Existencia de la tensión superficial
1º Experimento de Dupré.
Una cajita rectangular de cartón ABCD (ver figura 8) tiene una pared lateral CD móvil alrededor de su arista inferior C, por estar unida a la caja mediante una membrana elástica. Dicha pared está mantenida por un calce K y un hilo tirante DE. Se vierte agua hasta el borde del vaso. La presión hidrostática tiende a aplicar CD contra el calce, pero la tensión superficial que se ejerce sobre el borde superior D, según DA, tiende a acercar CD a la vertical. Esta última es más fuerte, pues si se quema el hilo DE, la pared CD tiende a aproximarse a la vertical, atraída según DA.
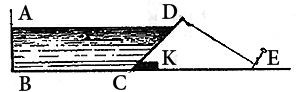
Figura 8: Tensión superficial
2º Experimento de Pasteur.
Cuando se hunde una varilla de cristal en un baño de mercurio espolvoreado con arena muy fina, se acercan a la varilla los granos de arena y desaparecen en torno suyo a medida que aquella se hunde. Cuando se retira la varilla, el polvo vuelve poco a poco a su puesto primitivo. Si se retira bruscamente la varilla, los granos saltan hasta cierta altura.
3º Experimento de Plateau.
Se prepara una mezcla de agua y alcohol que contenga exactamente la misma densidad que el aceite. El aceite puro introducido en dicha mezcla se sustrae a la gravedad en virtud del principio de Arquímedes. Obedece, pues, únicamente a las fuerzas de cohesión. Se observa que se reúne en forma exactamente esférica (ver figura 9), pues la tensión superficial es igual en todos los puntos de la superficie del aceite.

Figura 9: Experimento de Plateau
4º Una aguja o una hojita de afeitar colocadas cuidadosamente sobre la superficie del agua flotan formando un hueco debido a la tensión superficial.
5º Los insectos se desplazan sobre la superficie del agua.
6º La tensión superficial explica las pompas de jabón y la forma esférica de las gotas de agua.
7º La tensión superficial produce también la ascensión y depresión capilares.

Figura 10: Tensión superficial en la ascensión y depresión
En (1) la tensión superficial obra en la dirección de las fuerzas tangenciales T y T’, cuya resultante es R. Se establece el equilibrio cuando el peso P del agua que se ha elevado sea igual a R:
P = R
En (2) la tensión superficial actúa hacia abajo según T y T’. Hay equilibrio cuando la resultante R’ es igualada por una fuerza opuesta P’ (presión hidráulica):
P' = R'
Cálculo de la tensión superficial
En un tubo capilar de radio r = 0,05 cm el agua sube a 3 cm sobre el nivel exterior. ¿Cuál es la tensión superficial del agua?
Sea T la tensión que se ejerce en un centímetro de longitud.
El peso de la columna de líquido es:
π r2 h d g
La tensión que en la superficie del líquido lo eleva es:
2 π r T
Se igualan ambas expresiones.

La tensión superficial del agua es 73,5 dinas/cm; la del éter es 18 dinas/cm.
Términos destacados :
| English |
Español |
| capillarity | (capilaridad). Fenómeno por el cual un líquido asciende o desciende en tubos muy delgados debido a la acción de fuerzas intermoleculares. |
| capillary tube | (tubo capilar). Tubo de diámetro muy pequeño en el cual los líquidos no obedecen las leyes de los vasos comunicantes. |
| capillary rise | (ascensión capilar). Elevación del nivel de un líquido que moja las paredes de un tubo capilar. |
| capillary depression | (depresión capilar). Descenso del nivel de un líquido que no moja las paredes del tubo capilar. |
| meniscus | (menisco). Curvatura de la superficie libre de un líquido en contacto con un sólido, convexa o cóncava según la adherencia. |
| adhesion | (adherencia). Fuerza de atracción entre moléculas de sustancias distintas, como el agua y el vidrio. |
| cohesion | (cohesión). Fuerza de atracción entre moléculas de una misma sustancia. |
| Jurin's law | (ley de Jurín). Ley que establece que la altura alcanzada por un líquido en un tubo capilar es inversamente proporcional al diámetro del tubo. |
| Gay-Lussac method | (método de Gay-Lussac). Procedimiento experimental para comprobar la ley de Jurín usando tubos capilares de diferentes diámetros. |
| diffusion | (difusión). Fenómeno por el cual dos líquidos miscibles o gases se mezclan espontáneamente hasta formar una mezcla homogénea. |
| miscible liquids | (líquidos miscibles). Líquidos que pueden mezclarse completamente entre sí. |
| gas diffusion | (difusión de gases). Mezcla progresiva de gases debida al movimiento molecular y a diferencias de densidad. |
| Dalton's law of partial pressures | (ley de presiones parciales de Dalton). La presión total de una mezcla gaseosa es la suma de las presiones que ejercería cada gas si ocupara todo el volumen. |
| osmosis | (ósmosis). Paso de un líquido a través de una membrana porosa desde una solución menos concentrada hacia otra más concentrada. |
| endosmosis | (endósmosis). Entrada de agua a través de una membrana hacia el interior de una solución más concentrada. |
| exosmosis | (exosmosis). Movimiento del solvente hacia el exterior de una solución, disminuyendo inicialmente el nivel del líquido. |
| crystalloid | (cristaloide). Sustancia capaz de atravesar membranas porosas, como el azúcar disuelto en agua. |
| colloid | (coloide). Sustancia cuyas partículas no atraviesan membranas porosas, como el protoplasma o la clara de huevo. |
| osmotic pressure | (presión osmótica). Presión necesaria para detener el flujo osmótico del solvente a través de una membrana semipermeable. |
| manometer | (manómetro). Instrumento para medir presión, utilizado en experimentos de presión osmótica. |
| surface tension | (tensión superficial). Fuerza que actúa en la superficie libre de un líquido, haciéndola comportarse como una membrana elástica. |
| Dupré experiment | (experimento de Dupré). Experimento que demuestra la acción de la tensión superficial sobre superficies en contacto con líquidos. |
| Pasteur experiment | (experimento de Pasteur). Experimento que muestra la acción de la tensión superficial mediante una varilla sumergida en mercurio con polvo. |
| Plateau experiment | (experimento de Plateau). Demostración de que un líquido forma una esfera perfecta cuando su peso queda compensado por flotación. |
| floating needle | (aguja flotante). Fenómeno en el cual una aguja colocada cuidadosamente sobre agua puede flotar debido a la tensión superficial. |
| soap bubble | (pompa de jabón). Película líquida esférica estabilizada por tensión superficial. |
| capillary action | (acción capilar). Conjunto de fenómenos de ascenso o descenso de un líquido en tubos delgados. |
| meniscus curvature | (curvatura del menisco). Forma cóncava o convexa que adopta la superficie de un líquido por la acción combinada de cohesión y adherencia. |
| hydrostatic pressure | (presión hidrostática). Presión ejercida por un líquido en reposo, que interviene en fenómenos capilares. |
| specific gravity | (densidad relativa). Relación entre la densidad de una sustancia y la del agua, relevante en difusión y flotación. |
| communicating vessels | (vasos comunicantes). Principio según el cual los líquidos en recipientes conectados alcanzan el mismo nivel, excepto en tubos capilares. |
| free surface | (superficie libre). Superficie de un líquido en contacto con el aire, donde actúan las fuerzas de tensión superficial. |
| contact angle | (ángulo de contacto). Ángulo formado entre la superficie del líquido y la pared del tubo, determinante en el menisco. |
| density difference | (diferencia de densidad). Factor que influye en la difusión de gases y líquidos. |
| copper sulfate solution | (solución de sulfato de cobre). Mezcla obtenida por disolución del sulfato de cobre en agua durante la difusión. |
| homogeneous mixture | (mezcla homogénea). Mezcla uniforme que resulta de la difusión completa de dos sustancias. |
| membrane permeability | (permeabilidad de la membrana). Propiedad que determina qué sustancias pueden atravesarla durante la ósmosis. |
| porous membrane | (membrana porosa). Barrera con pequeños poros que permite el paso selectivo de líquidos durante la ósmosis. |
| hydrostatic equilibrium | (equilibrio hidrostático). Estado en el que las fuerzas debidas al peso del líquido se equilibran con otras fuerzas aplicadas. |
| capillary equilibrium | (equilibrio capilar). Condición en la cual la tensión superficial se compensa con el peso del líquido ascendido o deprimido. |
| tangential forces | (fuerzas tangenciales). Fuerzas que actúan a lo largo de la superficie del líquido debido a la tensión superficial. |
| resultant force | (fuerza resultante). Suma vectorial de las fuerzas de tensión superficial que equilibran el peso del líquido ascendido o descendido. |
| mercury column | (columna de mercurio). Parte del manómetro que se eleva o desciende según la presión osmótica. |
| graduated rod | (varilla graduada). Instrumento usado para medir la altura del líquido en el experimento de Jurín. |
| adhesive forces | (fuerzas adhesivas). Fuerzas que atraen el líquido hacia las paredes del tubo y generan meniscos cóncavos. |
| cohesive forces | (fuerzas cohesivas). Fuerzas internas del líquido que tienden a mantener su masa unida y generan meniscos convexos. |
| surface film | (película superficial). Capa delgada del líquido donde la tensión superficial se manifiesta con mayor intensidad. |
| sphere formation | (formación esférica). Tendencia de un líquido a adoptar forma de esfera para minimizar su superficie, como en el experimento de Plateau. |
| liquid column | (columna de líquido). Altura que alcanza un líquido por acción de la tensión superficial o la presión osmótica. |
| specific weight | (peso específico). Peso por unidad de volumen del líquido, involucrado en el cálculo de ascensión capilar. |
|