TERMODINÁMICA: Rama de las ciencias; trata con las relaciones entre el calor y la acción mecánica.
Los motores de combustión interna, tanto los de gasolina como los motores Diesel, funcionan gracias a la transformación de la energía contenida en el combustible. En estos motores el combustible líquido se pulveriza y se mezcla con el aire dentro de la cámara de combustión. En el caso del motor Diesel, el combustible es inyectado a presión en forma muy fraccionada, mientras que en el motor de gasolina la mezcla se produce previamente en el carburador antes de entrar al cilindro.
Durante el funcionamiento del motor los gases presentes en el interior del cilindro experimentan variaciones de presión, volumen y temperatura. En el ciclo de cuatro tiempos, el aire o la mezcla aire-combustible es admitido inicialmente a presión atmosférica y temperatura ambiente. Posteriormente se comprime dentro del cilindro, lo que provoca un aumento considerable de su presión y temperatura. Durante la combustión se generan temperaturas muy elevadas, y finalmente los gases se expulsan durante el tiempo de escape.
Para estudiar estas variaciones se utilizan representaciones gráficas llamadas diagramas termodinámicos. Uno de los más utilizados es el Este tipo de representación permite analizar cómo cambian las condiciones del gas dentro del cilindro durante el funcionamiento del motor.
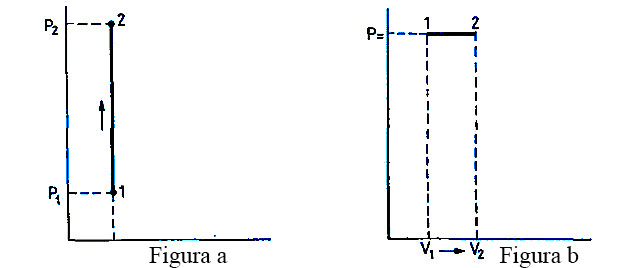
Figura a. Representación de una transformación isócora sobre un diagrama de Clapeyron. El volumen V es constante, pero la presión pasa de P1 a P2.
Figura b. Representación de una transformación isóbara sobre un diagrama de Clapeyron.
Dentro del estudio de la termodinámica se distinguen diferentes tipos de transformaciones que pueden experimentar los gases. Estas transformaciones describen cómo varían las variables fundamentales del estado de un gas, como la presión, el volumen y la temperatura.
Transformación isotérmica
La transformación isotérmica es aquella en la que la temperatura del gas permanece constante. En este tipo de proceso, cuando el volumen del gas disminuye, la presión aumenta, y viceversa. Esta relación está expresada por la conocida ley de Boyle o Mariotte, según la cual el producto entre la presión y el volumen permanece constante.
Este tipo de transformación puede representarse en el diagrama de Clapeyron mediante una curva característica que muestra cómo la presión aumenta a medida que el volumen disminuye manteniendo la temperatura constante.
Transformación isócora
La transformación isócora o isovolumétrica se produce cuando el volumen del gas permanece constante. En este caso, cualquier variación de temperatura se refleja directamente en una variación de presión. Este proceso puede presentarse cuando el pistón permanece inmóvil dentro del cilindro mientras se produce una combustión o un aporte de calor.
En este tipo de transformación la relación entre presión y temperatura es proporcional, siempre que el volumen permanezca fijo.
Transformación isóbara
En la transformación isóbara la presión del gas permanece constante mientras el volumen varía. Para que esta condición se mantenga es necesario que exista un aporte o una extracción de calor que compense las variaciones del volumen. Este tipo de proceso puede observarse en algunos momentos del funcionamiento de motores o en sistemas donde la presión del gas está regulada.
En este caso la temperatura absoluta del gas se relaciona directamente con el volumen, de modo que cuando el volumen aumenta también lo hace la temperatura.
Transformación adiabática
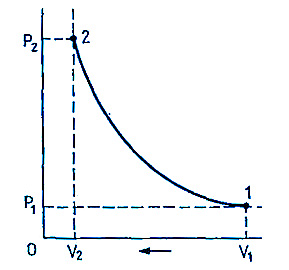
Figura : La temperatura absoluta varía en la siguiente relación:
\(
\frac{T_2}{T_1} =
\left(\frac{V_1}{V_2}\right)^{\gamma - 1}
\)
La transformación adiabática también se conoce con el nombre de transformación isentrópica, y así es nombrada en algunos tratados de Termodinámica.
La transformación adiabática se caracteriza porque no existe intercambio de calor con el exterior. En los motores de combustión interna, los procesos de compresión y expansión del gas se aproximan a este tipo de transformación. En una transformación adiabática la relación entre presión y volumen sigue una ley característica que depende del coeficiente adiabático del gas.
Este tipo de proceso también se conoce como transformación isentrópica en muchos textos de termodinámica, ya que ocurre sin transferencia de calor con el entorno.
Transformación politrópica
Finalmente, en la práctica real de los motores se observa que muchos procesos no son perfectamente adiabáticos ni isotérmicos. En estos casos se habla de una transformación politrópica. Este tipo de transformación representa con mayor precisión lo que ocurre dentro de los cilindros durante la compresión y expansión del gas, ya que puede existir cierta transferencia de calor durante el movimiento del pistón.
El estudio de estas transformaciones termodinámicas permite comprender con mayor claridad el comportamiento de los gases en los motores y constituye la base teórica para analizar su rendimiento y mejorar su diseño.
Los ciclos termodinámicos en los motores térmicos
En los motores térmicos, como los motores de combustión interna, las turbinas de gas y las máquinas de vapor, el funcionamiento se basa en una sucesión periódica de estados del gas caracterizados por diferentes valores de presión, volumen y temperatura. Esta serie de transformaciones que experimenta el gas dentro del motor se denomina ciclo termodinámico.
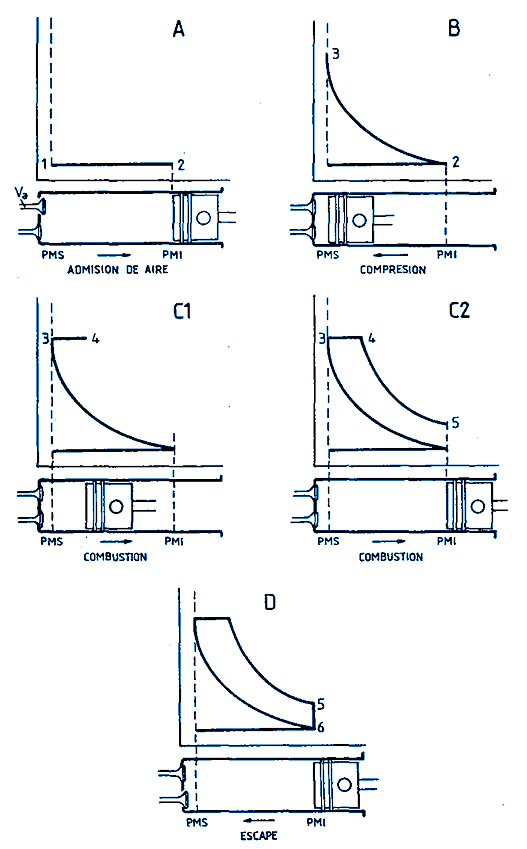
Figura : Diferentes fases del ciclo termodinámico de un motor Diesel representadas sobre un diagrama de Clapeyron.
Durante el funcionamiento del motor, el fluido de trabajo atraviesa distintas etapas en las cuales se modifican sus propiedades físicas. Estas transformaciones pueden representarse gráficamente mediante un diagrama de Clapeyron, también conocido como diagrama presión-volumen (P–V). En este tipo de gráfico se representa la presión del gas en el eje vertical y el volumen en el eje horizontal. El área encerrada por la curva del ciclo representa el trabajo realizado por el motor.
El análisis de estos diagramas permite comprender el comportamiento de los gases dentro del cilindro de un motor. En el caso del motor Diesel, el ciclo completo incluye varias fases que corresponden a los tiempos del motor: admisión, compresión, combustión y escape. Durante la admisión el aire entra en el cilindro a presión atmosférica. Luego, durante la compresión, el pistón reduce el volumen del gas, lo que provoca un aumento significativo de la presión y de la temperatura.
Cuando el pistón alcanza el punto muerto superior, se produce la inyección del combustible y la combustión dentro de la cámara. Durante esta etapa se generan presiones muy elevadas que impulsan el pistón hacia abajo, produciendo trabajo mecánico. Finalmente, durante el tiempo de escape, los gases quemados se expulsan del cilindro y el ciclo vuelve a comenzar.
La repetición continua de estas fases explica por qué se utiliza el término ciclo para describir el funcionamiento de los motores térmicos. Cada repetición del proceso produce una cantidad determinada de trabajo mecánico que es transmitido al cigüeñal del motor.
Desde el punto de vista teórico, uno de los ciclos termodinámicos más importantes es el ciclo de Carnot, que representa el modelo ideal de funcionamiento de una máquina térmica. Este ciclo está compuesto por cuatro transformaciones fundamentales: dos transformaciones isotérmicas y dos transformaciones adiabáticas.
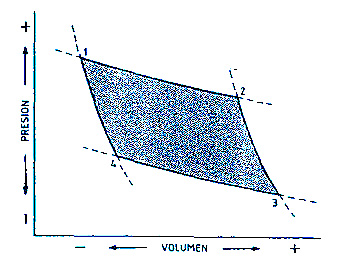
Figura : Ciclo de Carnot. De 1 a 2, expansión isotérmica. De 2 a 3, expansión adiabática. De 3 a 4, compresión isotérmica. De 4 a 1, compresión adiabática.
En la primera etapa se produce una expansión isotérmica, durante la cual el sistema absorbe calor de una fuente caliente mientras realiza trabajo. En la segunda etapa ocurre una expansión adiabática, donde el gas continúa expandiéndose sin intercambio de calor con el exterior. Posteriormente se produce una compresión isotérmica, en la cual el sistema cede calor al exterior mientras recibe trabajo mecánico. Finalmente tiene lugar una compresión adiabática que devuelve el sistema a su estado inicial.
El ciclo de Carnot es considerado un ciclo reversible ideal y establece el límite máximo de eficiencia que puede alcanzar una máquina térmica que opere entre dos temperaturas determinadas. Aunque los motores reales no pueden reproducir exactamente este ciclo ideal, su estudio resulta fundamental para comprender el rendimiento de los motores y las limitaciones impuestas por las leyes de la termodinámica.
A partir de las diferentes transformaciones termodinámicas —isotérmicas, isócoras, isóbaras y adiabáticas— se pueden construir diversos tipos de ciclos utilizados en máquinas térmicas. Entre los más importantes se encuentran los ciclos a temperatura constante, los ciclos a volumen constante, los ciclos a presión constante y otros ciclos aplicados a motores específicos. El análisis de estos ciclos permite diseñar motores más eficientes y comprender mejor el comportamiento energético de los sistemas térmicos.
Términos relacionados :
- 1. Termodinámica. (Thermodynamics)
- 2. Ciclo termodinámico. (Thermodynamic cycle)
- 3. Combustible líquido. (Liquid fuel)
- 4. Cámara de combustión. (Combustion chamber)
- 5. Inyector. (Fuel injector)
- 6. Gasóleo. (Diesel fuel)
- 7. Carburador. (Carburetor)
- 8. Mezcla aire-combustible. (Air–fuel mixture)
- 9. Gas de combustión. (Combustion gases)
- 10. Presión del gas. (Gas pressure)
- 11. Volumen del gas. (Gas volume)
- 12. Temperatura del gas. (Gas temperature)
- 13. Diagrama de Clapeyron. (Clapeyron diagram / P-V diagram)
- 14. Transformación termodinámica. (Thermodynamic transformation)
- 15. Transformación isotérmica. (Isothermal transformation)
- 16. Ley de Boyle-Mariotte. (Boyle–Mariotte law)
- 17. Transformación isócora. (Isochoric transformation)
- 18. Transformación isóbara. (Isobaric transformation)
- 19. Transformación adiabática. (Adiabatic transformation)
- 20. Transformación isentrópica. (Isentropic transformation)
- 21. Transformación politrópica. (Polytropic transformation)
- 22. Pistón o émbolo. (Piston)
- 23. Compresión del gas. (Gas compression)
- 24. Expansión del gas. (Gas expansion)
- 25. Ciclo de cuatro tiempos. (Four-stroke cycle)
|