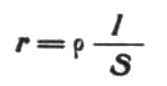|

|
Industrial Electrolysis of Brine
The industrial electrolysis of brine involves the decomposition of an aqueous sodium chloride solution into chlorine gas,
hydrogen gas, and sodium hydroxide. When dissolved in water, NaCl dissociates into sodium cations (Na+) and chloride
anions (Cl-). Under an applied voltage, chloride ions migrate to the anode where they are oxidized to chlorine gas
(Cl2), while water molecules at the cathode are reduced to hydrogen gas (H2) and hydroxide ions
(OH-). The Na+ and OH- then combine in solution to form caustic soda (NaOH).
A critical aspect of the process is the internal resistance of the electrolyte, which depends on ion concentration, electrode
spacing, and electrode surface area. This ohmic resistance, expressed as r = ρ · (l / S), must be overcome
along with the electrochemical counter-EMF generated by the reactions, resulting in a terminal voltage requirement given by
Vb = E + r·I.
Three primary cell technologies are used:
-
Mercury (Castner–Kellner) Cell:
Utilizes a flowing mercury cathode to form a sodium–mercury amalgam that is subsequently decomposed with water to yield
NaOH and regenerate mercury.
-
Diaphragm (Nelson) Cell:
Employs a porous diaphragm (often asbestos or polymer) to separate anodic and cathodic compartments, permitting
Na+ migration while preventing Cl- and OH- from mixing.
-
Membrane Cell:
Uses an ion-exchange membrane (e.g., PTFE-based) to selectively allow Na+ and water into the cathode chamber,
producing high-purity NaOH with lower energy consumption and minimal hazardous byproducts.
The overall stoichiometric reaction is:
2 NaCl(aq) + 2 H2O(l) → Cl2(g) + H2(g) + 2 NaOH(aq)
The co-production of chlorine, hydrogen, and caustic soda is central to many industries. Chlorine is widely used for water
disinfection, PVC production, and bleaching. Sodium hydroxide serves in pulp and paper processing, alumina refining, and
chemical manufacturing. Hydrogen finds applications as a clean energy carrier and in various chemical syntheses.
Environmental and safety considerations drive technology choice. Mercury cells have been phased out in many regions due to
toxic mercury emissions. Diaphragm cells remain in use but generate lower-purity NaOH. Membrane cells have become the global
standard, minimizing hazardous waste, reducing energy consumption, and producing high-purity caustic soda. These advances
underscore the ongoing evolution of chlor-alkali technology toward greater efficiency, sustainability, and safety.
|
| |
Producción de cloro por electrólisis de salmuera
Sea (fig. 1) una cuba electrolítica en la que se dispone como electrolito una disolución de sal común
(cloruro sódico) en agua. Cada molécula de cloruro sódico (NaCl) se disocia en los dos iones que la forman,
resultando iones positivos (cationes) de sodio (Na+) e iones negativos (aniones) de cloro (Cl-).
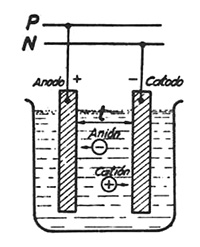
Figura 1. Cuba electrolítica
Introduciendo en el electrolito dos placas de platino conectadas a una fuente de energía eléctrica, éste será
atravesado por una corriente eléctrica. Las dos placas de platino son los electrodos: la positiva es el ánodo y la negativa
el cátodo.
La acción de la corriente eléctrica hace que los aniones de cloro se dirijan al ánodo y que los cationes de sodio se
depositen en la placa negativa o cátodo, siguiendo el sentido de la corriente.
Esta propiedad que tiene la corriente de transportar los metales al cátodo es aprovechada en numerosas e interesantes aplicaciones
(galvanoplastia, galvanostegia, electrometalurgia, etc.).
Resistencia interior del electrolito
Conforme con la teoría de la electrólisis, se deduce que únicamente pueden ser atravesadas por corriente eléctrica
las disoluciones que contienen iones. Por otra parte, el fenómeno de la corriente eléctrica en el seno de los electrolitos
es sustancialmente diferente del que se presenta en un conductor metálico.
En efecto, en los conductores metálicos o de primera clase, la corriente eléctrica se debe a un desplazamiento de
electrones desde un cuerpo cuyos átomos poseen exceso de electrones hasta otros cuyos átomos están a falta de ellos.
En cambio, en los electrolitos o conductores de segunda clase la corriente se debe al transporte de los iones que se encuentran
disociados.
Por consiguiente, debemos admitir que la resistencia opuesta por un electrolito al paso de la corriente eléctrica depende de la
cantidad de iones disociados, de la carga eléctrica que poseen y de su velocidad de traslación. Prácticamente es
siempre impreciso el cálculo de la resistencia interior de un electrolito. Su valor, de acuerdo con la fórmula, es:
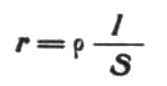
Siendo S la superficie media de los electrodos, l la distancia que los separa y ρ la
resistividad del electrolito, valor que depende de las características de los iones disociados.
La resistividad ρ del electrolito y, por consiguiente, la resistencia interior r varían con la
temperatura, como sucede con los conductores metálicos. Ahora bien, entre aquéllos y éstos se presenta otra diferencia
fundamental.
Como ya vimos, la resistencia de un conductor metálico aumenta al crecer la temperatura y se reduce al disminuir ésta. En
cambio, en un electrolito sucede a la inversa: su resistencia disminuye al aumentar la temperatura. Esto se debe a que al aumentar la
temperatura de un electrolito crece el número de iones disociados y aumenta su velocidad de traslación, efectos ambos que
hacen disminuir la resistencia del electrolito.
Este es el motivo de que en los baños de galvanoplastia y galvanostegia se trabaje siempre con temperaturas superiores a
las del ambiente, a fin de acelerar los resultados que se desean conseguir.
Fuerza contraelectromotriz
Experimentalmente se comprueba que en un baño de resistencia interior r, para que circule una corriente de
I amperios de intensidad, no basta con aplicarle una tensión V = r·I, sino que la tensión
en bornes ha de ser mayor que este valor. Ello se debe a que en el baño aparece una fuerza contraelectromotriz, por lo que la
tensión necesaria en los bornes del baño será:
Vb = E + r·I
La fuerza contraelectromotriz E no es otra cosa que la parte de la tensión necesaria para producir los fenómenos
químicos, siendo r·I la caída de tensión interior.
La electrólisis se refiere a la descomposición de una sustancia por una corriente eléctrica. La electrólisis de
hidróxidos de sodio y de potasio, llevada a cabo por primera vez en 1808 por Sir Humphry Davy, condujo al descubrimiento de estos
dos elementos metálicos y mostró que estos dos hidróxidos, que anteriormente habían sido considerados
indescomponibles y, por lo tanto, elementos, estaban de hecho compuestos.
Equivalente electroquímico
Recibe el nombre de equivalente electroquímico de una sustancia el peso, en miligramos, de la misma depositado en un proceso de
electrólisis por la cantidad de electricidad de un culombio o, lo que es igual, por una corriente eléctrica de un amperio de
intensidad durante un segundo de tiempo.
Representaremos el equivalente electroquímico por la letra griega ε (se lee "épsilon").
En la Tabla I siguiente aparecen los equivalentes electroquímicos de las sustancias más corrientes.
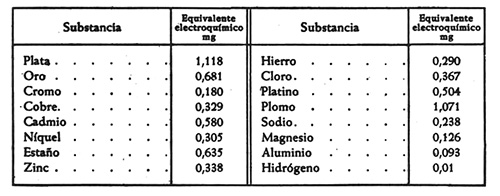
Tabla I. Equivalentes electroquímicos
La electrólisis de salmuera es una tecnología para producir sosa cáustica y cloro a partir de la sal, que es uno de
los minerales más comunes en la Tierra.
Es ampliamente reconocido que la sosa cáustica se usa como material para la producción de aluminio y vidrio, y el cloro para
desinfectar el agua. La sosa cáustica y el cloro son productos químicos básicos e importantes utilizados en una amplia
gama de industrias, como la producción de plásticos, la industria textil, la pulpa, el aluminio, el acero y el refinamiento
de petróleo. El hidrógeno es un subproducto de este proceso.
La salmuera es una solución de cloruro de sodio (NaCl) y agua (H2O). El proceso de electrólisis implica el uso de una
corriente eléctrica para provocar un cambio químico y formar nuevos productos. La electrólisis de salmuera es un proceso
a gran escala utilizado para la fabricación de cloro a partir de la sal. Otros dos productos útiles se obtienen durante el
proceso: hidróxido de sodio (NaOH) e hidrógeno (H2).
En resumen:
- El hidróxido de sodio, NaOH, también se conoce como lejía o sosa cáustica.
- El hidróxido de sodio es una base de uso común.
-
La electrólisis de soluciones concentradas de cloruro de sodio (salmuera) produce gas cloro, gas de hidrógeno e
hidróxido de sodio acuoso.
2NaCl(aq) + 2H2O(l) → H2(g) + Cl2(g) + 2NaOH(aq)
Es importante que el cloro y el hidróxido de sodio producidos en el proceso se separen, ya que reaccionan cuando entran en contacto
entre sí.
Cl2(g) se produce en el ánodo (electrodo positivo).
H2(g) y NaOH(aq) se producen en el cátodo (electrodo negativo).
Usos en la industria
Los productos de la electrólisis de salmuera tienen usos importantes en la industria. Algunos de estos usos se encuentran en la
tabla de abajo, pero hay muchos más.
Productos resultantes de la electrólisis de salmuera:
| |
Usos del producto químico |
| Cloro |
Desinfectante y purificador.
Fabricación de ácido clorhídrico.
Fabricación de plásticos.
|
| Hidróxido de sodio |
Procesamiento de productos alimenticios.
Eliminación de contaminantes del agua.
Fabricación de papel.
|
| Hidrógeno |
Fabricación de ácido clorhídrico.
Potencial como combustible no contaminante.
|
| |
Propiedades del producto químico |
| Cloro |
Gas venenoso amarillo. |
| Hidróxido de sodio |
Base fuerte.
Soluble en agua.
La disolución de NaOH en agua es una reacción exotérmica.
Delicuescente: absorbe la humedad del aire.
Absorbe dióxido de carbono del aire.
|
| Hidrógeno |
Gas inflamable. |
Los impactos ambientales de la electrólisis de salmuera a gran escala deben ser considerados. El proceso utiliza una gran cantidad
de electricidad, que se produce principalmente por la quema de combustibles fósiles. Durante el proceso real de la electrólisis,
un metal debe estar en contacto con la solución de salmuera. Un metal comúnmente usado es el mercurio, que es tóxico.
Algo de mercurio puede escapar hacia la solución y al medio ambiente.
Tres tipos de celda electrolítica se utilizan para producir hidróxido de sodio a partir de la salmuera:
- Celda Castner–Kellner (proceso de mercurio)
- Celda de diafragma de Nelson
- Celda de membrana
Celda Castner–Kellner (proceso de mercurio)

Ánodo (electrodo positivo): titanio.
Ánodo, reacción (oxidación):
2Cl-(aq) → Cl2(g) + 2e-
Cátodo (electrodo negativo): mercurio que fluye a lo largo de la parte inferior de la celda.
Cátodo, reacción (reducción):
Na+(aq) + e- → Na(s)
El Na(s) se disuelve en el mercurio líquido para formar una amalgama que se retira al descomponedor.
En el descomponedor, la amalgama reacciona con el agua para formar hidróxido de sodio, gas hidrógeno y mercurio:
2Na/Hg + 2H2O(l) → 2Na+ + 2OH- + H2(g) + 2Hg(l)
Se recogen solución de hidróxido de sodio y gas hidrógeno.
El mercurio se recicla a través de la celda electrolítica.
Celda de diafragma de Nelson
Un diafragma poroso de amianto o de óxido de metal con polímero separa los compartimientos anódico y catódico.

El diafragma impide que los iones hidroxilo entren en el compartimiento del ánodo y evita que los iones cloruro entren en el
compartimiento del cátodo.
La salmuera saturada entra en el compartimiento del ánodo, donde se produce gas cloro.
Ánodo (electrodo positivo): carbono (grafito) o titanio recubierto con óxido de Ru–Ti.
Ánodo, reacción (oxidación):
2Cl-(aq) → Cl2(g) + 2e-
El Na+ migra a través del diafragma al compartimiento del cátodo, combinándose con OH- para formar NaOH.
Reacción celular general (mostrando iones espectadores Na+):
2H2O(l) + 2Cl-(aq) + 2Na+(aq)
→ 2Na+(aq) + 2OH-(aq) + H2(g) + Cl2(g)
El producto contiene cloruro de sodio e hidróxido de sodio. El NaOH(s) se puede cristalizar.
Celda de membrana

Es el método preferido para la producción de hidróxido de sodio, ya que no deja residuos peligrosos, produce
hidróxido de sodio muy puro y tiene los requisitos de energía más bajos.
La membrana de intercambio iónico permite selectivamente que el Na+ y el agua fluyan hacia el compartimiento del
cátodo, pero impide que los productos se muevan entre los compartimientos.
La salmuera saturada entra en el compartimiento del ánodo, donde se forma el gas cloro.
Ánodo (electrodo positivo): titanio.
Ánodo, reacción (oxidación):
2Cl-(aq) → Cl2(g) + 2e-
Cátodo (electrodo negativo): níquel.
Cátodo, reacción (reducción):
2H2O(l) + 2e- → H2(g) + 2OH-(aq)
El Na+ migra a través de la membrana al compartimiento del cátodo, combinándose con OH- para formar NaOH.
Reacción celular general (mostrando iones espectadores Na+):
2H2O(l) + 2Cl-(aq) + 2Na+(aq)
→ 2Na+(aq) + 2OH-(aq) + H2(g) + Cl2(g)
El producto es hidróxido de sodio concentrado.
Una celda de membrana puede considerarse una celda de diafragma con un separador mejorado (la "membrana"). Suele fabricarse con
politetrafluoroetileno (PTFE), es decir, un plástico muy inerte, modificado para incluir grupos aníonicos que actúan como
sitios de intercambio iónico. Esto permite que los iones de sodio pasen a través de ella, pero no los iones cloruro ni los
iones hidroxilo. Por lo tanto, las reacciones ocurren como en la celda de diafragma, pero sin subproducto significativo de cloruro de sodio,
ya que la membrana evita la mezcla entre cloruro e hidroxilo.
El uso de este proceso produce hidróxido de sodio prácticamente puro (por ejemplo, puede contener aproximadamente 0,02% de
cloruro de sodio, como máximo) y reduce riesgos laborales asociados al amianto o al mercurio.
Este proceso ha sido adoptado en muchas plantas de cloro-álcali debido a su alta pureza de hidróxido de sodio, costos
razonables y un impacto ambiental significativamente menor. En la práctica, el proceso de membrana ha demostrado ser la técnica
más conveniente para la producción de hidróxido de sodio.
La industria de cloro-álcali (también llamada "cloro cáustico") es una de las mayores tecnologías
electroquímicas del mundo. Es un proceso de alto consumo energético y se encuentra entre los mayores consumidores de electricidad
dentro de las industrias electrolíticas.
El cloro se produce por electrólisis de una solución de cloruro de sodio (sal de mesa común), a menudo llamada
"salmuera". Cuando el NaCl se disuelve en agua, se disocia en cationes sodio y aniones cloruro. Los iones cloruro se oxidan en el
ánodo para formar gas cloro y las moléculas de agua se reducen en el cátodo para formar iones hidroxilo y gas hidrógeno.
Los iones sodio en la solución y los iones hidroxilo producidos en el cátodo constituyen los componentes del hidróxido de
sodio formado durante la electrólisis.

Figura: Sala de celdas de cloro-álcali con celdas de diafragma MDC-55 (Cortesía de Occidental Chemical Corporation)

Figura: Sala de celdas de cloro-álcali con celdas de membrana BL-2.7 (Cortesía de Uhde GmbH)
El cloro se produce electrolíticamente usando tres tipos de celdas electrolíticas. La diferencia principal entre estas
tecnologías se encuentra en la forma en que se impide que el gas cloro y el hidróxido de sodio se mezclen, a fin de asegurar la
generación de productos puros. En las celdas de diafragma, la salmuera del compartimiento del ánodo fluye a través del
separador hacia el compartimiento del cátodo; el separador puede ser amianto modificado con polímero u otros materiales porosos,
depositados sobre un cátodo perforado. En las celdas de membrana, se utiliza una membrana de intercambio iónico como separador.
En cambio, las celdas de mercurio no contienen diafragma ni membrana: el propio mercurio actúa como separador.
El ánodo, en todas las tecnologías modernas, es de titanio recubierto con una capa electrocatalítica de óxidos
mixtos. Muchas celdas modernas (desde la década de 1970) emplean los llamados "ánodos dimensionalmente estables" (DSA).
Las celdas anteriores utilizaban ánodos basados en carbono. El cátodo es típicamente de acero en las celdas de diafragma,
de níquel en las celdas de membrana, y de mercurio en las celdas de mercurio.
Tratamiento y purificación de la salmuera para uso a gran escala
La sal cruda, en su lugar de almacenamiento, se disuelve en agua caliente en el lixiviador (recipiente donde la sal y el agua se mezclan
para formar la salmuera). Se requiere salmuera de muy alta pureza para el proceso de electrólisis, especialmente para proteger las
membranas. Las impurezas presentes en la sal, en particular los compuestos de calcio y de magnesio, se eliminan por precipitación
química y filtración. La purificación final se lleva a cabo en columnas de intercambio iónico.
Conceptos destacados :
| brine ( industrial chemistry – electrochemistry ) |
(salmuera). Solución acuosa concentrada de cloruro de sodio utilizada como electrolito en el proceso cloro-álcali. |
| brine electrolysis ( industrial chemistry – electrochemistry ) |
(electrólisis de salmuera). Proceso electroquímico que descompone NaCl(aq) para obtener cloro, hidrógeno e hidróxido de sodio. |
| chlor-alkali process ( industrial chemistry – electrochemistry ) |
(proceso cloro-álcali). Tecnología industrial para producir Cl₂, H₂ y NaOH por electrólisis de salmuera. |
| sodium chloride (NaCl) ( chemistry – electrochemistry ) |
(cloruro de sodio). Sal que en disolución se disocia en iones Na⁺ y Cl⁻. |
| aqueous solution ( chemistry ) |
(disolución acuosa). Mezcla donde el agua actúa como solvente de los solutos iónicos. |
| dissociation ( chemistry – electrochemistry ) |
(disociación). Separación de NaCl en iones Na⁺ y Cl⁻ al disolverse en agua. |
| cation ( chemistry – electrochemistry ) |
(catión). Ion con carga positiva, como Na⁺, que migra hacia el cátodo. |
| anion ( chemistry – electrochemistry ) |
(anión). Ion con carga negativa, como Cl⁻, que migra hacia el ánodo. |
| electrolyte ( electrochemistry ) |
(electrolito). Disolución que contiene iones móviles capaces de conducir corriente eléctrica. |
| electrolytic cell ( electrochemistry – industrial chemistry ) |
(cuba electrolítica). Dispositivo donde una fuente externa aplica tensión para forzar reacciones electroquímicas. |
| electrode ( electrochemistry ) |
(electrodo). Conductor en contacto con el electrolito donde ocurren oxidación o reducción. |
| anode ( electrochemistry ) |
(ánodo). Electrodo donde ocurre la oxidación; en salmuera se forma cloro. |
| cathode ( electrochemistry ) |
(cátodo). Electrodo donde ocurre la reducción; se produce hidrógeno y OH⁻. |
| oxidation ( electrochemistry ) |
(oxidación). Pérdida de electrones; por ejemplo, 2Cl⁻ → Cl₂ + 2e⁻ en el ánodo. |
| reduction ( electrochemistry ) |
(reducción). Ganancia de electrones; por ejemplo, 2H₂O + 2e⁻ → H₂ + 2OH⁻ en el cátodo. |
| chlorine gas (Cl₂) ( industrial chemistry – electrochemistry ) |
(gas cloro). Producto anódico obtenido por oxidación de iones cloruro. |
| hydrogen gas (H₂) ( industrial chemistry – electrochemistry ) |
(gas hidrógeno). Producto catódico obtenido por reducción del agua. |
| sodium hydroxide (NaOH) ( industrial chemistry – electrochemistry ) |
(hidróxido de sodio, sosa cáustica). Producto que se forma en solución por combinación de Na⁺ y OH⁻. |
| hydroxide ion (OH⁻) ( electrochemistry ) |
(ion hidróxido). Ion generado en el cátodo durante la reducción del agua. |
| terminal voltage ( electrical engineering – electrochemistry ) |
(tensión en bornes). Tensión necesaria para vencer la f.c.e.m. y la caída óhmica: Vb = E + r·I. |
| electrochemical counter-EMF ( electrical engineering – electrochemistry ) |
(fuerza contraelectromotriz). Parte de la tensión requerida para producir las reacciones químicas. |
| internal resistance ( electrical engineering – electrochemistry ) |
(resistencia interior). Resistencia del electrolito que depende de concentración iónica, distancia y área de electrodos. |
| resistivity (ρ) ( electrical engineering ) |
(resistividad). Propiedad del electrolito que determina la resistencia según r = ρ·(l/S). |
| ohmic resistance ( electrical engineering – electrochemistry ) |
(resistencia óhmica). Caída de tensión por conducción iónica en el electrolito, proporcional a r·I. |
| diaphragm cell (Nelson cell) ( industrial chemistry – electrochemical engineering ) |
(celda de diafragma). Celda con separador poroso que permite el paso de Na⁺ pero evita la mezcla de Cl⁻ y OH⁻. |
| membrane cell ( industrial chemistry – electrochemical engineering ) |
(celda de membrana). Celda con membrana de intercambio iónico que produce NaOH de alta pureza y menor consumo energético. |
| mercury cell (Castner–Kellner cell) ( industrial chemistry – electrochemical engineering ) |
(celda de mercurio). Tecnología que usa mercurio como cátodo para formar amalgama Na-Hg y luego producir NaOH. |
| amalgam ( industrial chemistry – electrochemistry ) |
(amalgama). Aleación de sodio con mercurio formada en la celda de mercurio. |
| ion-exchange membrane ( materials science – electrochemical engineering ) |
(membrana de intercambio iónico). Membrana selectiva que permite el paso de Na⁺ y restringe Cl⁻ y OH⁻. |
|