English  |
Español  |
| battery ( Refrigeration and HVAC Components - Thermodynamic and Physical Concepts - Measuring Instruments and Control Devices ) |
BATERÍA: Celdas productoras de electricidad, que funcionan por la interacción de metales y químicos para crear un flujo de corriente eléctrica. |
| battery (Automotive) |
Batería, acumulador.

Requisitos y Adecuación de la Batería del Vehículo.
La batería del vehículo sirve como una fuente crucial de energía cuando el motor, y en consecuencia el alternador, no están operativos. Para cumplir su función de manera efectiva, la batería del vehículo debe cumplir varios requisitos, que se describen a continuación en un orden general de importancia:
Almacenamiento de Energía y Suministro Rápido:
La batería debe almacenar suficiente energía y ser capaz de entregarla rápidamente para operar el motor de arranque del vehículo.
Uso Prolongado de Luces de Estacionamiento:
Debe permitir el uso de las luces de estacionamiento durante un tiempo razonable sin agotar excesivamente la energía.
Operación de Accesorios:
La batería debe permitir el funcionamiento de accesorios, como radios o luces interiores, cuando el motor no está en marcha.
Estabilidad de Voltaje:
La batería debe actuar como un amortiguador para absorber y amortiguar las fluctuaciones en el voltaje del sistema del vehículo, asegurando un rendimiento eléctrico estable.
Mantenimiento de Memoria Dinámica y Sistemas de Alarma:
Debe mantener la energía para los sistemas de memoria y alarmas, permitiendo que sigan activos incluso cuando el vehículo se deja desatendido durante un período largo.
Los dos primeros requisitos mencionados anteriormente se consideran altamente críticos y juegan un papel importante en la determinación de la batería más adecuada para una aplicación específica. Hasta ahora, las baterías de plomo-ácido, disponibles en varias formas similares, han demostrado ser la opción más apropiada para las aplicaciones de vehículos, especialmente cuando se considera su rentabilidad.

Además, la batería del vehículo debe cumplir todas las funciones mencionadas anteriormente en un amplio rango de temperaturas. Este rango puede variar desde aproximadamente 30 hasta 70 grados Celsius, abarcando condiciones extremadamente frías para el arranque, así como temperaturas elevadas bajo el capó del vehículo.
Asegurarse de que la batería cumpla con estos requisitos es esencial para un funcionamiento confiable del vehículo y un rendimiento óptimo. La batería de plomo-ácido ha demostrado su compatibilidad con estas demandas, lo que la convierte en una opción popular y confiable para el uso en vehículos.
Tecnología de Baterías de Automóviles y Electroquímica.
El ámbito de la tecnología de baterías está estrechamente relacionado con el campo de la electroquímica. Específicamente, se centra en el estudio de las celdas galvánicas y la electrólisis. Cuando un electrolito se somete a una corriente eléctrica, provoca reacciones químicas específicas y fomenta el movimiento de materiales. Bajo ciertas condiciones, las reacciones químicas particulares pueden generar energía eléctrica utilizando la energía libre presente dentro del sistema. Las reacciones más interesantes son aquellas que poseen reversibilidad, es decir, que pueden convertir energía eléctrica en energía química y viceversa. Para comprender mejor este dominio, es útil familiarizarse con varios términos y conceptos. A continuación, se presentan algunos términos esenciales y sus explicaciones concisas:
- Anión: Es un ion cargado negativamente que migra hacia el terminal positivo durante el proceso de electrólisis.
- Ánodo: Designa el electrodo positivo de una celda.
- Catalizador: Un catalizador es una sustancia que mejora significativamente la velocidad de una reacción química sin participar activamente en ella.
- Catión: Representa un ion cargado positivamente que se mueve hacia el terminal negativo durante la electrólisis.
- Cátodo: El cátodo denota el electrodo negativo de una celda.
- Difusión: Caracteriza la mezcla autoimpulsada de líquidos o gases.
- Disociación: Significa la descomposición de moléculas o átomos en una solución, resultando en la formación de iones positivos y negativos. Por ejemplo, cuando el ácido sulfúrico (H2SO4) se disocia, se descompone en H+ y H+ (dos iones positivos o cationes atraídos hacia el cátodo) y SO42- (iones negativos o aniones atraídos hacia el ánodo).
- Electrodo: Se refiere a las placas encontradas en las baterías o en los baños de electrólisis, los cuales están suspendidos dentro del electrolito.
- Electrólisis: Se refiere a la conducción de electricidad entre dos electrodos sumergidos en una solución electrolítica, lo que provoca cambios químicos en los electrodos.
- Electrolito: Es un líquido conductor de iones que rodea ambos electrodos.
- Ion: Un ion es una partícula, ya sea atómica o molecular, que lleva una carga positiva o negativa.
- Celda galvánica secundaria: Este tipo de celda incluye electrodos y un electrolito. Durante la carga, convierte la energía eléctrica en energía química, y durante la descarga, experimenta el proceso inverso.
Al comprender estos términos, se puede profundizar en el fascinante mundo de la tecnología de baterías y la electroquímica.
Conducción Electrolítica y Flujo de Iones.
La transmisión de electricidad a través de conductores puede ocurrir mediante dos mecanismos distintos. El primer método involucra el movimiento de electrones, observado predominantemente en la mayoría de las sustancias metálicas. El segundo modo de conducción se basa en el movimiento iónico, en el cual los átomos o moléculas cargadas sirven como conductores. Para que la electricidad atraviese un electrolito, el flujo de iones se vuelve esencial.
Para explicar el concepto de conducción electrolítica, consideremos el ejemplo del ácido sulfúrico (H2SO4) como un electrolito ejemplar, especialmente cuando se disuelve en agua. Cuando esto ocurre, el ácido sulfúrico se disocia, resultando en la formación de H+ (iones de hidrógeno), H+ (más iones de hidrógeno) y SO42- (iones sulfato), que poseen cargas positivas y negativas. Los iones cargados positivamente se atraen hacia el electrodo negativo, mientras que los iones cargados negativamente se atraen hacia el electrodo positivo. Este movimiento de iones se conoce comúnmente como flujo iónico o deriva iónica.
Términos destacados :
- Anión (Anion)
- Catalizador (Catalyst)
- Celda galvánica secundaria (Secondary galvanic cell)
- Conducción electrolítica (Electrolytic conduction)
- Difusión (Diffusion)
- Disociación (Dissociation)
- Electrolito (Electrolyte)
- Electrólisis (Electrolysis)
- Flujo iónico (Ion flow)
- Ánodo (Anode)
En resumen, la conducción electrolítica involucra el paso de corriente eléctrica a través de un medio líquido. Utilizando el ácido sulfúrico como ejemplo ilustrativo de electrolito, el proceso de flujo iónico ocurre a medida que los iones positivos y negativos migran hacia sus respectivos electrodos. Este fenómeno subyace en el mecanismo fundamental de transmisión de electricidad en sistemas electrolíticos. |
| battery (e.g. 12V automotive) (Automotive) |
Batería. Combinación de pilas conectadas de forma que produzcan energía eléctrica útil. Celdas productoras de electricidad, que funcionan por la interacción de metales y químicos, para crear un flujo de corriente eléctrica. (small battery, e.g. 1.5V) Pila. (Ver recursos relacionados)


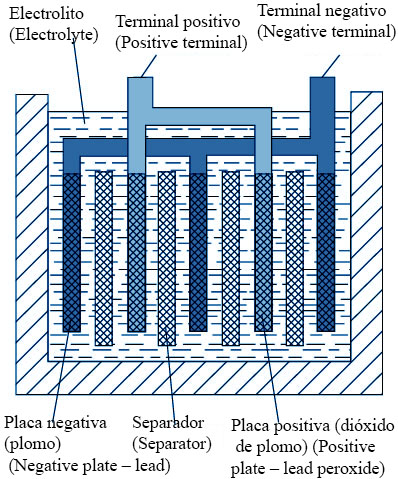
Electrolito (Electrolyte)
Terminal positivo (Positive terminal)
Terminal negativo (Negative terminal)
Placa negativa (plomo) (Negative plate – lead)
Separador (Separator)
Placa positiva (dióxido de plomo) (Positive plate – lead peroxide)
Figura : Batería de automóvil
Las baterías utilizadas en motocicletas y vehículos todo terreno (ATV) son, en su mayoría, baterías de plomo-ácido, diseñadas para almacenar energía eléctrica en forma química y entregarla cuando el sistema lo requiere. Su función principal es suministrar corriente para el arranque del motor, alimentar los sistemas eléctricos y estabilizar la tensión del circuito.
Una batería convencional está compuesta por una carcasa que contiene varias celdas. Cada celda posee placas positivas de dióxido de plomo y placas negativas de plomo esponjoso, separadas por separadores aislantes e inmersas en un electrolito formado por una solución de ácido sulfúrico y agua destilada. La reacción química entre las placas y el electrolito permite almacenar y liberar energía. Al conectarse varias celdas en serie se obtiene la tensión total de la batería.
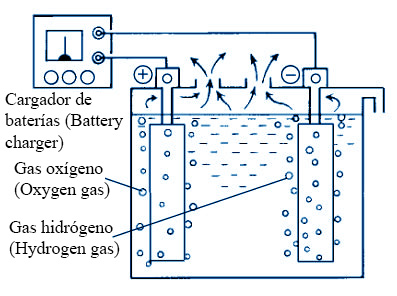
Fig. : Cuando una batería se está cargando, se produce una reacción química que presuriza la batería. Asegúrese de retirar los tapones de ventilación de la batería al cargarla.;
Cargador de baterías (Battery charger)
Gas oxígeno (Oxygen gas)
Gas hidrógeno (Hydrogen gas)
Durante el proceso de descarga, la batería entrega corriente al circuito y se forman compuestos de sulfato de plomo en ambas placas, reduciéndose la concentración del ácido. En la carga, suministrada por el sistema eléctrico del vehículo, estas reacciones se invierten, restaurando las características químicas originales. Si se aplica una corriente excesiva, el electrolito se calienta y se produce evaporación de agua, generando gases; por esta razón, las baterías convencionales poseen tapones de ventilación y requieren control periódico del nivel de electrolito.
Las baterías libres de mantenimiento son una evolución de las convencionales. Están selladas, consumen menos agua y presentan menor emisión de gases. Aunque reducen las tareas de servicio, no están exentas de fallas y deben ser inspeccionadas regularmente.
La inspección de baterías incluye la verificación del estado de la carcasa, limpieza de bornes y control de cables. La presencia de sulfato, corrosión o conexiones flojas provoca pérdidas de corriente y mal funcionamiento del sistema de arranque. Un método habitual de diagnóstico es la medición de la densidad del electrolito con un hidrómetro, que permite estimar el estado de carga. Una densidad alta indica batería cargada; valores bajos señalan descarga o deterioro.
El mantenimiento adecuado implica mantener el nivel correcto de electrolito, usar únicamente agua destilada, asegurar una carga apropiada y evitar descargas profundas prolongadas. Una batería descargada o en mal estado reduce su vida útil y puede afectar seriamente el rendimiento del vehículo.
Resumiendo concetpos, la batería es un componente esencial del sistema eléctrico. Su correcto funcionamiento depende de su diseño interno, del control químico durante la carga y descarga, y de una inspección periódica que garantice fiabilidad, seguridad y larga vida útil.
Términos relacionados :
Batería de plomo-ácido (Lead-acid battery)
Batería convencional (Conventional battery)
Batería libre de mantenimiento (Maintenance-free battery)
Bornes / terminales (Terminals)
Carcasa (Casing)
Celda (Cell)
Placas (Plates)
Placa positiva (Positive plate)
Placa negativa (Negative plate)
Separador (Separator)
Electrolito (Electrolyte)
Agua destilada (Distilled water)
Ácido sulfúrico (Sulfuric acid)
Tapón de ventilación (Vent cap)
Orificio de ventilación (Vent)
Gases de carga (Gassing)
Carga de batería (Battery charging)
Descarga de batería (Battery discharging)
Hidrómetro (Hydrometer)
Gravedad específica (Specific gravity)
|
| battery (Electric Current and Charge Transport) |
(batería). Fuente electroquímica capaz de suministrar energía eléctrica de forma continua.
Baterías y fuentes de energía eléctrica portátil
Las baterías constituyen uno de los elementos fundamentales en los sistemas electrónicos modernos, ya que permiten almacenar energía química y convertirla en energía eléctrica de manera controlada. Su uso se extiende desde dispositivos portátiles pequeños, como controles remotos y relojes, hasta aplicaciones más exigentes como vehículos eléctricos, sistemas de respaldo y equipos industriales.
Existen diferentes tipos de baterías, que pueden clasificarse principalmente en baterías primarias y baterías secundarias. Las baterías primarias son aquellas que no pueden recargarse, ya que sus reacciones químicas internas son irreversibles. Ejemplos comunes incluyen las baterías alcalinas, de zinc-carbón y de litio no recargables. Por otro lado, las baterías secundarias son recargables y permiten múltiples ciclos de carga y descarga, como las de plomo-ácido, níquel-cadmio (NiCd), níquel-hidruro metálico (NiMH) y litio-ion (Li-ion).
Una batería está compuesta por una o más celdas electroquímicas, cada una formada por un ánodo, un cátodo y un electrolito. Durante la descarga, se produce una reacción química que genera un flujo de electrones desde el ánodo hacia el cátodo a través del circuito externo. Este flujo es el que alimenta el dispositivo conectado.
Las características más importantes de una batería incluyen su voltaje nominal, su capacidad (generalmente expresada en miliamperios-hora, mAh), su resistencia interna y su vida útil. El voltaje nominal depende del tipo de química utilizada, mientras que la capacidad indica cuánta energía puede almacenar la batería. La resistencia interna influye en la caída de tensión bajo carga, y la vida útil está relacionada con el número de ciclos de carga y descarga que puede soportar.
En el mercado existen múltiples formatos físicos de baterías, como las conocidas AA, AAA, C, D y tipo botón. Cada formato tiene aplicaciones específicas según el tamaño, la capacidad y la corriente requerida. Por ejemplo, las baterías AA son muy utilizadas en dispositivos domésticos, mientras que las baterías tipo botón se emplean en relojes y dispositivos pequeños.
Las baterías de litio-ion han ganado gran popularidad debido a su alta densidad energética, bajo peso y capacidad de recarga. Sin embargo, requieren sistemas de control electrónico para evitar sobrecargas, descargas profundas y sobrecalentamiento. Estos sistemas de protección son esenciales para garantizar la seguridad y prolongar la vida útil de la batería.
En aplicaciones más grandes, como sistemas de respaldo energético (UPS) o automóviles, se utilizan baterías de plomo-ácido. Estas baterías son robustas, relativamente económicas y capaces de entregar altas corrientes. Sin embargo, son más pesadas y tienen menor densidad energética que las baterías modernas de litio.
Otro aspecto importante es el comportamiento de la batería frente a la descarga. A medida que una batería se descarga, su voltaje tiende a disminuir. La curva de descarga depende del tipo de batería y de las condiciones de uso. Algunas baterías mantienen un voltaje relativamente constante durante gran parte de su descarga, mientras que otras presentan una caída más pronunciada.
La temperatura también influye significativamente en el rendimiento de las baterías. A bajas temperaturas, la capacidad disponible disminuye debido a la reducción de la actividad química. A altas temperaturas, puede aumentar la eficiencia momentáneamente, pero se acelera el desgaste y el envejecimiento de la batería.
En cuanto a la recarga, cada tipo de batería requiere un método específico. Por ejemplo, las baterías de NiCd y NiMH pueden tolerar ciertos niveles de sobrecarga, mientras que las de litio-ion requieren un control preciso de tensión y corriente. Los cargadores modernos incorporan circuitos inteligentes que regulan el proceso de carga para optimizar el rendimiento y evitar daños.
Además, es importante considerar el impacto ambiental de las baterías. Algunos tipos contienen materiales tóxicos, como el cadmio o el plomo, que requieren una disposición adecuada. Por esta razón, se promueve el reciclaje de baterías y el desarrollo de tecnologías más ecológicas.
Las especificaciones técnicas de las baterías suelen presentarse en tablas que incluyen parámetros como voltaje, capacidad, corriente máxima, temperatura de operación y dimensiones físicas. Estas tablas permiten seleccionar la batería adecuada para cada aplicación.
En sistemas electrónicos, el diseño de la fuente de alimentación debe tener en cuenta no solo la capacidad de la batería, sino también la estabilidad del voltaje, la eficiencia energética y la protección contra fallas. En muchos casos, se utilizan reguladores de tensión para mantener un suministro constante independientemente del estado de carga de la batería.
En aplicaciones portátiles, la eficiencia energética es crítica. Dispositivos como teléfonos móviles, laptops y sensores inalámbricos dependen de baterías de alta eficiencia y bajo consumo. Por ello, el diseño electrónico busca minimizar el consumo y optimizar el uso de la energía disponible.
En base a lo visto, las baterías son una pieza clave en la electrónica moderna, permitiendo la portabilidad y autonomía de los dispositivos. Su selección y uso adecuado requieren comprender sus características, limitaciones y comportamiento bajo distintas condiciones. La evolución tecnológica continúa mejorando su rendimiento, seguridad y sostenibilidad, lo que las convierte en un área de gran importancia en la ingeniería eléctrica y electrónica.
Estilos de encapsulado y características típicas de baterías
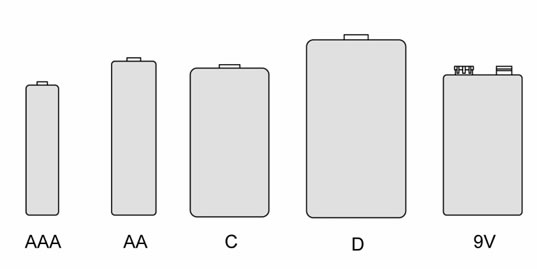
| Tipo de batería |
AAA |
AA |
C |
D |
9 V |
| Tensión nominal - Alcalina |
1,5 V |
1,5 V |
1,5 V |
1,5 V |
9 V |
| Tensión nominal - NiCad |
1,2 V |
1,2 V |
1,2 V |
1,2 V |
8,4 V |
| Tensión nominal - NiMH |
1,2 V |
1,2 V |
1,2 V |
1,2 V |
8,4 V |
| Capacidad típica - Alcalina |
1200 mAh |
1800 mAh |
7500 mAh |
17000 mAh |
550 mAh |
| Capacidad típica - NiCad |
350 mAh |
600 mAh |
2500 mAh |
5000 mAh |
120 mAh |
| Capacidad típica - NiMH |
800 mAh |
600 mAh |
4500 mAh |
9500 mAh |
200 mAh |
Nota: Las capacidades son aproximadas y pueden variar según el fabricante de la batería y el tipo (estándar o de alta capacidad).
Conceptos clave
- Batería primaria (Primary battery)
- Batería secundaria (Secondary battery)
- Celda electroquímica (Electrochemical cell)
- Voltaje nominal (Nominal voltage)
- Capacidad (Capacity)
- Resistencia interna (Internal resistance)
- Densidad energética (Energy density)
- Ciclo de carga/descarga (Charge/discharge cycle)
- Curva de descarga (Discharge curve)
- Batería de litio-ion (Lithium-ion battery)
- Batería de plomo-ácido (Lead-acid battery)
- Sistema de protección (Protection circuit)
- Corriente de carga (Charging current)
- Voltaje de salida (Output voltage)
- Regulación de tensión (Voltage regulation)
- Eficiencia energética (Energy efficiency)
- Temperatura de operación (Operating temperature)
- Reciclaje de baterías (Battery recycling)
- Formato de batería (Battery size/format)
- Fuente de alimentación portátil (Portable power supply)
|
 
|
